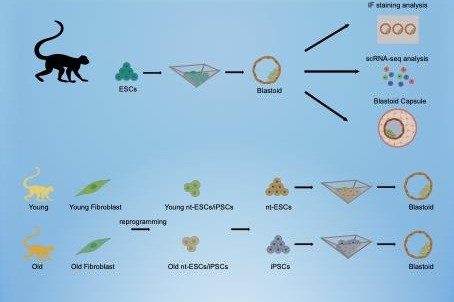
به گزارش چاینا دیلی، این بلاستوئیدها، ساختارهای شبهجنینی تولیدشده در شرایط آزمایشگاهی هستند که مراحل اولیه رشد جنین را شبیهسازی میکنند و میتوانند به عنوان مدلهای حیاتی برای مطالعه رشد جنینی و درمانهای بازسازیکننده مورد استفاده قرار گیرند.
بلاستوئید ساختاری آزمایشگاهی است که از سلولهای بنیادی مشتق میشود و شباهت زیادی به بلاستوسیست، یعنی یکی از مراحل اولیه رشد جنین در پستانداران، دارد. برخلاف بلاستوسیست واقعی که از لقاح طبیعی تخمک و اسپرم بهوجود میآید، بلاستوئیدها از سلولهای بنیادی پرتوان، مانند سلولهای بنیادی جنینی یا سلولهای بنیادی پرتوان القایی، در محیط آزمایشگاه تولید میشوند. این ساختارها قادرند مرحله اولیه رشد جنینی را شبیهسازی کنند، بدون آنکه نیازی به سلولهای جنسی یا لقاح طبیعی باشد. همچنین، چون در شرایط آزمایشگاهی تولید میشوند، قابلیت کنترل، تکرار و مهندسی شدن بالایی دارند.
بلاستوئیدها نقش مهمی در تحقیقات زیستپزشکی ایفا میکنند. آنها امکان مطالعه دقیق و اخلاقی مراحل اولیه رشد جنین را بدون نیاز به استفاده از جنینهای واقعی فراهم میکنند. این قابلیت، فرصتی ارزشمند برای پیشرفت در پزشکی ترمیمی به شمار میآید، چرا که شناخت عملکرد سلولها در آغاز رشد میتواند به بازسازی اندامهای آسیبدیده کمک کند. همچنین، این ساختارها میتوانند به عنوان مدلهایی برای بررسی ناباروری، سقطهای مکرر و ناهنجاریهای جنینی مورد استفاده قرار گیرند.
علاوه بر آن، بلاستوئیدها بستری برای آزمون ایمنی و اثربخشی داروهای جدید در مراحل اولیه رشد جنین فراهم میسازند و امکان بررسی دقیق عملکرد ژنها و تأثیر ویرایشهای ژنتیکی را نیز فراهم میآورند.
در مجموع، بلاستوئیدها ابزارهای پیشرفتهای در حوزه زیستشناسی رشد و پزشکی نوین هستند. آنها افقهای تازهای برای درک بهتر فرایندهای حیاتی اولیه، توسعه درمانهای نوآورانه و بهکارگیری فناوریهای جدید در ترمیم و بازسازی بافتها میگشایند.
این پروژه توسط پژوهشگران دانشگاه علوم و فناوری کونمینگ در استان یوننان انجام شد. آنها با بهرهگیری از سلولهای بنیادی پرتوان القایی میمون و سلولهای بنیادی جنینی حاصل از انتقال هسته سلول سوماتیک، موفق به تولید بلاستوئیدهایی شدند که نرخ موفقیت تشکیل آنها به ۸۰ درصد رسید. در نمونههایی که از سلولهای میمونهای مسنتر استفاده شد، این میزان نیز به ۶۰ درصد رسید؛ دستاوردی که افقهای تازهای را در فهم بازسازی بافتها در سنین بالا میگشاید.
از دیگر نوآوریهای این تیم، توسعه یک پلتفرم میکروفلوئیدیک پیشرفته بود که با استفاده از زیستمواد، قادر به تولید کپسولهای بلاستوئیدی با ابعاد قابل تنظیم و تجزیهپذیر است. این سامانه میتواند تا ۴۰۰۰ کپسول در ساعت تولید کند و ساختاری سهبعدی و پایدار را فراهم میآورد که بازده انتقال به لوله فالوپ را به شکل چشمگیری افزایش میدهد؛ عاملی که نقش مهمی در کارایی بالینی آن خواهد داشت.
از مزایای کلیدی این روش میتوان به استانداردسازی و مقیاسپذیری فرآیند تولید بلاستوئیدها اشاره کرد، که گامی مهم بهسوی استفاده عملی و گستردهتر از آنها در حوزههای درمانی و تحقیقاتی به شمار میرود.
با وجود این پیشرفتها، دانشمندان تأکید کردند که هنوز نیاز به بهینهسازی بیشتر وجود دارد؛ بهویژه در زمینه بهبود عملکرد سلولهای تروفوبلاست موجود در کپسولها. برنامهریزی برای مطالعات آتی نیز شامل بهبود شرایط کشت، توسعه مواد زیستی نوین و بررسی رشد بلندمدت کپسولهای بلاستوئیدی در بدن موجود زنده است.
این پژوهش نهتنها مسیرهای جدیدی را برای مطالعه رشد جنینی و بیماریهای مرتبط باز میکند، بلکه زمینهساز تحولی چشمگیر در کاربردهای آینده پزشکی ترمیمی خواهد بود. کارشناسان بر این باورند که با ادامه توسعه این فناوری، بلاستوئیدهای مهندسیشده میتوانند نقشی کلیدی در تحقیقات زیستپزشکی پیشبالینی ایفا کنند.
تولید بلاستوئیدهای میمون از طریق سلولهای بنیادی مزایای چشمگیری برای حوزههای مختلف علمی و پزشکی به همراه دارد و مسیرهای نوینی را برای پیشرفت در زیستپزشکی و پزشکی ترمیمی میگشاید. این نوع تحقیقات امکان شبیهسازی مراحل اولیه رشد جنین را بدون استفاده از جنینهای واقعی فراهم میکند، که از نظر اخلاقی و عملی یک دستاورد مهم به شمار میآید. از جمله مهمترین فواید آن میتوان به توسعه مدلهای دقیق برای مطالعه رشد جنینی، درک بهتر از دلایل ناباروری و ناهنجاریهای رشدی، و آزمون ایمنی داروهای جدید اشاره کرد.
این دستاورد همچنین در پزشکی ترمیمی نقش کلیدی ایفا میکند، زیرا میتواند به بازسازی اندامها و بافتهای آسیبدیده بهویژه در افراد مسن کمک کند. موفقیت تیم تحقیقاتی در استفاده از سلولهای میمونهای مسنتر و رسیدن به نرخ تشکیل ۶۰ درصدی بلاستوئیدها، افقهای تازهای در بازسازی بافت در فرآیند پیری گشوده است. علاوه بر این، توسعه پلتفرم میکروفلوئیدیک نوینی که قادر به تولید سریع و پایدار کپسولهای بلاستوئیدی با ساختار سهبعدی و قابلیت تجزیهپذیری است، گامی مهم در مسیر استانداردسازی و مقیاسپذیری این فناوری محسوب میشود؛ امری که استفاده بالینی و گستردهتر از این ابزارهای زیستی را ممکن میسازد.
در مجموع، این نوع تحقیقات نهتنها ابزارهای نوینی برای مطالعه دقیقتر رشد جنینی و بیماریهای مرتبط فراهم میآورد، بلکه بستری مهم برای توسعه روشهای درمانی بازسازیکننده در آینده است. استمرار این پژوهشها میتواند جایگاه بلاستوئیدهای مهندسیشده را به عنوان ابزاری محوری در تحقیقات پیشبالینی و پزشکی نوین تثبیت کند.
منبع: chinadaily