به گزارش چاینا دیلی، این پژوهش مشترک توسط مؤسسه تحقیقاتی در هانگژو و دانشگاه علوم و فناوری جنوبی در شنژن انجام شده و نتایج آن در نشریه معتبر منتشر شده است.
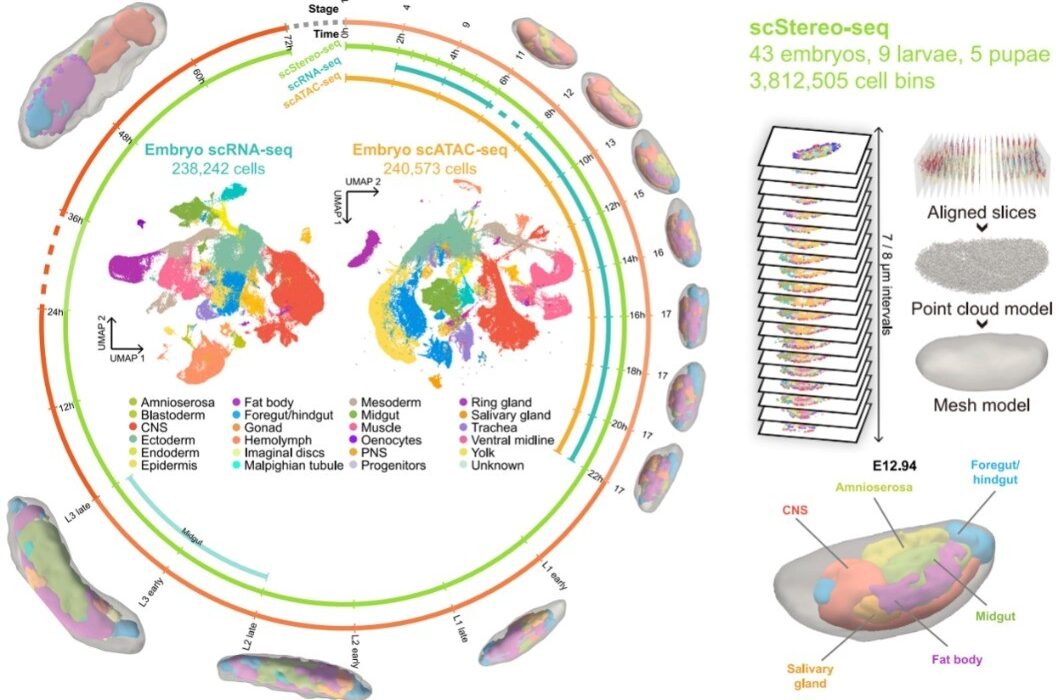
در این مطالعه، رشد مگس میوه – به عنوان یک ارگانیسم مدل – بهدقت از چهار مرحله مشخص تخم، لارو، شفیره و بالغ بررسی شد. دانشمندان با استفاده از فناوریهای پیشرفته، نمونهبرداری متراکم از جنینها را در فواصل ۳۰ دقیقه تا ۲ ساعت انجام دادند و دادههایی با دقت بالا از مراحل مختلف رشد جمعآوری کردند.
نتیجه این پروژه، تولید یک پایگاه داده عظیم با بیش از ۳.۸ میلیون رونوشت سلول منفرد بود که امکان بازسازی یک مدل سهبعدی دقیق از دینامیک مکانی و زمانی رشد بافتها و بیان ژن را فراهم کرد. ابزار الگوریتمی پیشرفته برای تحلیل این دادهها به کار گرفته شد.
دادههای بهدستآمده به پژوهشگران این امکان را داد تا نقشهای از مسیر تمایز سلولی ترسیم کرده و مکانیسمهای مولکولی حاکم بر سرنوشت سلولها را شناسایی کنند. به گفتهی “وانگ مینگیو”، یکی از نویسندگان این مقاله، سلولهای لایههای مختلف زایا مسیرهای متمایزی را دنبال میکنند که تحت نظارت دقیق عوامل رونویسی قرار دارند. این عوامل نقش «مدیران سلولی» را ایفا میکنند و با تنظیم ژنها، فرآیند تمایز سلولها را کنترل میکنند.
وی افزود که در این مطالعه چندین عامل رونویسی جدید شناسایی شدهاند که میتوانند نقش کلیدی در تکامل سیستم عصبی، دستگاه گوارش و غدد درونریز ایفا کنند.
وانگ خاطرنشان کرد که حدود ۷۰ درصد از ژنهای دخیل در بیماریهای انسانی دارای همتایانی در مگسهای میوه هستند؛ بنابراین این پژوهش میتواند به عنوان مرجعی قدرتمند برای مطالعات زیستپزشکی و بررسی بیماریهای رشدی انسان مورد استفاده قرار گیرد.
این دستاورد، چشماندازهای تازهای برای درک رشد سلولی، درمان اختلالات ژنتیکی و پیشبرد پزشکی ترمیمی فراهم میآورد.
فواید و مزایای این اکتشاف علمی، چندلایه، بنیادین و فراتر از دنیای حشرات است و میتواند تحولی اساسی در درک ما از رشد زیستی و بیماریهای انسانی ایجاد کند. این پژوهش با ارائه یک اطلس سهبعدی دقیق از کل چرخه زندگی مگس میوه، امکان بررسی جزئیات شکلگیری، تکامل و تمایز سلولها را در سطح تکسلولی فراهم میسازد. چنین دادههایی شناخت عمیقتری از نحوهی کنترل ژنتیکی و زمانی فرآیندهای حیاتی موجودات زنده ارائه میدهند.
از آنجا که حدود ۷۰ درصد از ژنهای مرتبط با بیماریهای انسانی، در مگس میوه نیز وجود دارند، این یافتهها به مدلسازی دقیق بیماریهای رشدی، عصبی و غدد درونریز کمک کرده و مسیر تحقیقات درمانی را هدفمندتر میسازند. همچنین شناسایی عوامل رونویسی ناشناخته که در رشد دستگاه عصبی، گوارش و سیستم غدد نقش دارند، زمینهساز ابداع درمانهای نوین میشود.
نقشههای تمایز سلولی حاصل از این مطالعه میتوانند سلولهای بنیادی را در آزمایشگاه به انواع بافتی خاص هدایت کنند که این امر، یکی از بنیانهای اصلی پزشکی بازساختی و ژنتیک درمانی است. علاوه بر این، این پروژه بستری برای توسعه و آزمون ابزارهای تحلیلی پیشرفته فراهم کرده که کاربرد گستردهای در تحلیل دادههای زیستی دارند. دادههای دقیق دربارهی سلولهای زایا و مسیرهای تمایز آنها، امکان کشفیات عملی در زمینهی علوم اعصاب، غدد درونریز و زیستشناسی رشد را نیز فراهم میکند. در مجموع، این دستاورد علمی نهتنها مرجع جدید و ارزشمندی در زیستشناسی رشد محسوب میشود، بلکه افقهای تازهای برای پژوهشهای زیستپزشکی، ژنتیک و درمان بیماریهای انسانی میگشاید.
بسیاری از بیماریهای انسانی که با رشد، تمایز سلولی یا عملکرد ژنتیکی مرتبط هستند، میتوانند از چنین اکتشافاتی بهطور مستقیم یا غیرمستقیم بهرهمند شوند. برای نمونه، اوتیسم بهعنوان یک اختلال رشدی عصبی، اغلب ناشی از تمایز نادرست سلولهای عصبی در دوران جنینی است و دادههای مربوط به شکلگیری سلولهای عصبی در مگس میوه میتواند به درک بهتر آن کمک کند. در دیستروفی عضلانی که نتیجه نقص در ژنهای کنترلکننده عضلات است، بررسی مسیرهای تمایز عضلانی در مدلهای حیوانی، راه را برای درمانهای هدفمند هموار میسازد.
در مورد بیماری پارکینسون نیز، که با مرگ تدریجی نورونها همراه است، مطالعه چگونگی تمایز و زوال این سلولها میتواند به طراحی راهکارهای توقف یا حتی بازگرداندن عملکرد عصبی کمک کند. برخی انواع صرع ژنتیکی نیز با اختلال در بیان ژنها و تمایز سلولهای عصبی در ارتباطاند و شناخت دقیقتر این مسیرها امکان ژندرمانی مؤثر را فراهم میسازد. سرطانهایی مانند سرطان روده، مغز و تیروئید که با اختلال در مسیرهای تمایز سلولی شکل میگیرند نیز میتوانند با شناسایی مکانیزمهای جهشیافته از طریق چنین مطالعاتی، هدف درمانهای جدید قرار گیرند.
همچنین، درک دقیقتر رشد جنینی و مسیرهای سلولی میتواند در پیشگیری یا تشخیص زودهنگام نقایص مادرزادی مانند اسپینا بیفیدا یا مشکلات قلبی مؤثر واقع شود. حتی در بیماریهایی نظیر دیابت نوع یک که با تخریب سلولهای بتای پانکراس همراه است، شناخت مسیرهای تمایز این سلولها، امکان تولید و پیوند آنها در شرایط آزمایشگاهی را فراهم میکند. در مجموع، هر بیماری که ریشه در اختلال رشد، تمایز یا تنظیم ژنتیکی سلولها دارد، میتواند از دادههای حاصل از چنین اطلسهای زیستی و مدلسازیهای دقیق بهرهمند شود و در مسیر درمان یا پیشگیری، گامهای موثرتری بردارد.
منبع: chinadaily